目次
1.アフリカ豚コレラウイルス(ASFV)感染拡大の長い歴史
2.なぜ、これまで、アフリカ豚コレラウイルス(ASFV)に対するワクチンが開発されてこなかったのか?
(1)異なる3つの圏域での異なる3つの感染シナリオ
A.アフリカのアフリカ豚コレラ(ASF)感染圏域
B.ヨーロッパのアフリカ豚コレラ(ASF)感染圏域
C.東アジアのアフリカ豚コレラ(ASF)感染圏域
(2)アフリカ豚コレラウイルス(ASFV)自体の特異性
A. 特殊なアフリカ豚コレラウイルス(ASFV)の構造
B.巨大なウイルスと血球吸着現象
C.ウイルスの侵入から新たなウイルスの複製に至るまでの過程が複雑
D.様々な数と種類の構造タンパク質、それらをコードする遺伝子との結びつき関係が多様すぎる
(A)前駆体蛋白由来生成の成熟タンパク質(前駆体蛋白「pp220とpp62」由来生成の成熟タンパク質)
(B)抗原タンパク質「p54とp30とp72」
(C)糖タンパク質「CD2v」
(D)その他の主要タンパク質
E.数多い遺伝子型
(A)三種類もある遺伝子型配列クレード(系統樹)
(B)クレード(clade)(系統樹)決定の手順
(3)アフリカ豚コレラウイルス(ASFV)の免疫回避の動き
A.不十分な中和抗体生成への誘導と発現
B.免疫応答回避のための機序(evasion mechanisms)
(A)アップ・レギュレーションとダウン・レギュレーション
(B)アフリカ豚コレラウイルス(ASFV)侵入経路での免疫回避の動き
a.サイトカインの放出、b.ケモカインの放出、c.アポトーシスの阻害と、オートファジーの阻害、d.好中球の発現とリンパ球&単球、e.膜融合( membrane fusion)の阻害、f.転写活性体の応答低下、g.インターフェロンの働き、h.シグナル伝達(signaling pathway)の阻害、i.リン酸化酵素によるウイルス核内移行の促進とサイトカイン等の産生促進、j.MHCクラスI抗原の表面発現の阻害、k.樹状細胞によるサイトカイン応答調整
3.アフリカ豚コレラウイルス(ASFV)ワクチン開発の歴史と現状
(1)散々な失敗に終わった世界最初の最初のアフリカ豚コレラワクチン
(2)その後も続いたアフリカ豚コレラ(ASF)ワクチン開発の失敗
①不活化ワクチン(Inactivated vaccines)、②弱毒生ワクチン(Live attenuated vaccines, LAVs)、③サブユニットワクチン(Subunit vaccines)、④DNAワクチン(DNA vaccines)、⑤ウイルスベクター生ワクチン(Live virus-vectored vaccines)、⑥組み換え弱毒生ワクチン(Recombinant LAVs)
(3)中国へのアフリカ豚コレラ(ASF)感染拡大で勢いづく、世界のワクチン開発競争
A.潮目が変った、世界のASFVワクチン開発への動き
B.各国の動向
C.現在開発中の世界の研究機関は?
D.現在、アフリカ豚コレラワクチン開発に興味を有している民間企業は?
(4)現在、世界で最も有望なアフリカ豚コレラ(ASF)ワクチンはなにか?
A,ワクチン開発のための六条件
B.その中での有望な三例
(A)スペイン マドリッドコンプルテンス大学獣医学部での経口ワクチン開発
(B)アメリカ USDA プラム・アイランド動物疾病センターでのワクチン開発
(C)中国の中国農業科学院 ハルビン獣医研究所でのワクチン開発
4.終わりに
1.アフリカ豚コレラウイルス(ASFV)感染拡大の長い歴史
アフリカ豚コレラウイルスが東アジアに初めて侵入したのは、2018年8月3日、中国 遼寧省瀋陽市であった。
その後、アフリカ豚コレラは、中国国内一巡後、モンゴル(2019年1月9日)、ベトナム(2019年2月1日)、カンボジア(2019年3月22日)、香港(2019年5月2日)、北朝鮮(2019年5月23日)、ラオス(2019年6月2日)、フィリピン(2019年7月25日)、ミャンマー(2019年8月1日)、韓国(2019年9月17日)、東ティモール民主共和国(2019年9月9日)、インドネシア・北スマトラ州(2019年11月9日)へと感染拡大を続けている。
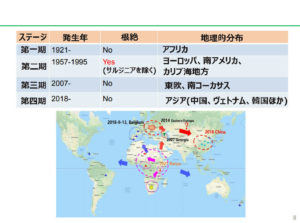
一方、ヨーロッパ大陸へのアフリカ豚コレラ ウイルスの上陸は、二期に分かれる。
第一期は、1957年から1990年半ばにかけての侵入であり、第二期は、2006年末から2007年にかけての東ヨーロッパへの侵入である。
第一期の時は、ポルトガル(1957年、1960年から1994年,1999年)、スペイン(1960年から1995年),フランス(1964年),イタリア(1967年、1969年、1993年),サルジニア島(1978年)、マルタ(1978年),ベルギー(1985年)、オランダ(1985年)に侵入し、1999年に、サルジニア島を残し、ようやく撲滅を果たした。
第二期の侵入は、東ヨーロッパから始まり、2006年末からのジョージアへの侵入が最初と言われている。
その後、アルメニア(2007年8月)、ロシア(2007年11月)、アゼルバイジャン(2008年1月)、ウクライナ(2012年7月30日)、ベラルーシ(2013年6月19日)、リトアニア(2014年1月24日)、ポーランド(2014年2月13日)、ラトビア(2014年6月)、エストニア(2014年9月)、モルドバ(2016年9月17日)、チェコ(2017年6月27日、2019年4月19日に清浄化宣言)、ルーマニア(2017年7月27日)、ハンガリー(2018年4月20日)、ブルガリア(2018年8月31日)、ベルギー(2018年9月9日)、スロバキア(2019年7月23日)、セルビア(2019年7月30日)
へと、今なお、拡大を続けている。
中米と南米では、キューバ(1971年)、ブラジル(1978年)、ドミニカ共和国(1978年)、ハイチ(1979年)に発生している。
アフリカでは、ケニアでのモンゴメリーによる1921年の発見(1909年には存在したとする説も)が最初だが、元々は、1700年代に、その祖先はいたと見られている。
以来、南アフリカ(1928年)、アンゴラ(1933年)と続き、風土病化した形で、サハラ砂漠以南の29カ国で発生しており、一旦終息した国でも、感染媒介ダニ・サイクルの特性故に、いまだに間歇的な発生を見せている国もある。
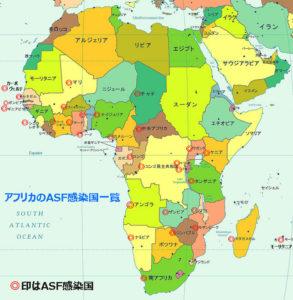
アフリカでのアフリカ豚コレラ ウイルス(ASFV)発生国は現在(2019年12月5日時点)は下記のとおりである。
アンゴラ(2009年)、ベナン(2005年)、ブルキナファソ(2005年)、ブルンジ(2005年)、カーボヴェルデ(2012年)、カメルーン(2012年)、中央アフリカ(2011年まで報告)、チャド(2012年)、コンゴ民主共和国(2005年)、コンゴ共和国(2009年)、ガーナ(2005年)、ガンビア(2011年)、ギニアビサウ(2005年)、ケニア(2012年)、マダガスカル(2005年)、マラウイ(2005年)、マリ(2009年)、モザンビーク(2005年)、ナミビア(2005年)、ナイジェリア(2005年)、ルワンダ(2005年)、セネガル(2005年)、シェラレオネ(2012年)、南アフリカ(2012年)、タンザニア(2005年)、トーゴ(2005年)、ウガンダ(2005年)、ザンビア(2005年)、ジンバブエ(2004年まで報告)、
参考
「Invasive Species Compendium African swine fever」
(CAB I(Centre for Agriculture and Bioscience International) )
2.なぜこれまでASFVワクチンが開発されてこなかったのか?
これ程の長い、しかも広範囲での感染の歴史をもつアフリカ豚コレラ(ASF)だが、このウイルスに対するワクチンは未だ開発されていない。
それにはいくつかの理由がある。
(1)異なる3つの圏域での異なる3つの感染シナリオ
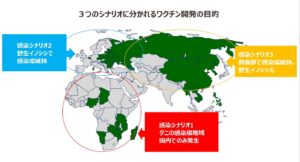
第一は、発生圏域におけるウイルスの宿主がそれぞれ異なり、したがって感染シナリオと言うべきものが、それぞれ異なり、ワクチン開発戦略の絞り込みができないことにある。
現在の世界の感染域は、下図の3つの圏域に分けられる。
それぞれの圏域における感染シナリオは下記のとおりである。
A.アフリカのアフリカ豚コレラ(ASF)感染圏域
アフリカにおけるアフリカ豚コレラウイルス(ASFV)は、森林サイクル(Sylvatic cycle)に基づいて、発生したり終息したりしている。
アフリカでは、野生のイボイノシシ(warthog)やカワイノシシ(河猪) (African bush pig)やモリイノシシ(Giant forest hog) が、アフリカ豚コレラウイルス(ASFV)に対し耐性を持ち、風土病化して生息している。
アフリカに於いてアフリカ豚コレラウイルスを媒介するのはダニの仲間のヒメダニ属のオルニトドロス(Ornithodorus.moubata )であり、これがASFウイルスの媒介に深く関与している。
このダニは普段は地中にいて、巣穴の近くのイノシシを吸血する際に地上に出てき、吸血が済んだら地中に戻るというサイクルを繰り返している。
そのため、ウイルスに感染したダニが豚を吸血することによって感染拡大はするが、その感染拡大範囲は、国内の範囲にとどまる。
また、巣窟に寄生する好熱性かつ疎光性のダニなので、あまり広範囲には広がらない。
したがって、アフリカでのアフリカ豚コレラ(ASF)は、感染スポットが孤立したまま、森林サイクル(Sylvatic cycle)での垂直的感染にとどまってきたと見られる。
まさに、アフリカでのアフリカ豚コレラ(ASF)感染は、ドメスティックの問題にとどまってきた。
それ故、アフリカ以外の国々の研究者にとつては、自国の利害と直結しないアフリカのためのワクチン開発としてとらえられ、ワクチン開発へのインセンティブが働いてこなかったのである。
B.ヨーロッパのアフリカ豚コレラ(ASF)感染圏域
ヨーロッパにおけるアフリカ豚コレラウイルスの感染拡大には、野生イノシシによる感染拡大が一定程度 寄与している。
その中で飼養豚への感染拡大阻止を図らなければならない。
陸地で感染国と接している非感染国は戦戦兢兢の状況を迫られている。
したがって、アフリカ豚コレラウイルスの感染拡大阻止のためには、感染した野生イノシシのコントロールが必要になる。
また、アフリカとは異なるダニ(オルニソドロス・エラティカス(Ornithodoros erraticus))が感染拡大に寄与している。
C.東アジアのアフリカ豚コレラ(ASF)感染圏域
東アジアにおけるアフリカ豚コレラウイルスの感染拡大は、飼養豚の感染拡大が主であり、それに一部、野生イノシシの感染媒介が加わる。
中国での飼養豚の感染拡大の原因として、飼養衛生管理の不徹底のほか、「泔水喂猪」(泔水(食堂の残飯・残滓)を飼料にして育てられた豚)による感染拡大や、感染肉の隠蔽・密売による感染拡大もあった。
更には、感染肉が、ソーセージなどの豚肉製品に混入され、移出・輸出され、感染拡大につながった例もある。
上記これらのアフリカ豚コレラ発生圏域の感染シナリオの違いが、これまで、アフリカ豚コレラ(ASF)ワクチンの開発を鈍らせてきたと言える。
(備考)
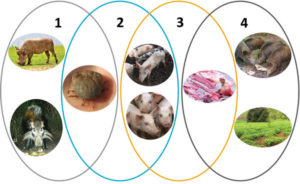
下記図ではアフリカ豚コレラに関する4つのサイクルがあるとしている。
1)シルバティック・サイクル
イボイノシシ、ブッシュピッグとダニとの間の感染サイクル
2)ダニと飼養豚のサイクル
ダニと飼養豚との間の感染サイクル
3)国内サイクル
国内飼養豚および豚由来製品(豚肉、血液、脂肪、ラード、骨、骨髄、皮)との間の感染サイクル。
4)野生イノシシの生息地でのサイクル
感染野生イノシシ由来の肉製品や感染イノシシ由来の死体や感染イノシシ生息地由来の感染などの間での感染サイクル。
参考「Identification of Wild Boar–Habitat Epidemiologic Cycle in African Swine Fever Epizootic」(Erika Chenais, Karl Ståhl, Vittorio Guberti,
Klaus Depner、2018年)
(2)アフリカ豚コレラウイルス(ASFV)自体の特異性
第二のワクチン開発遅延の理由は、以下に見るような、アフリカ豚コレラウイルス(ASFV)自体の特性にある。
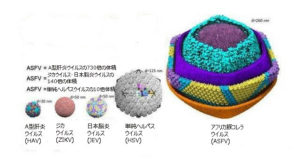
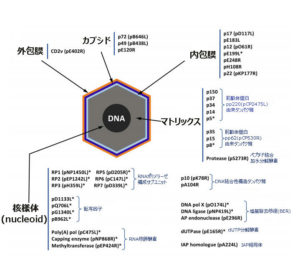
A. 特殊なアフリカ豚コレラウイルス(ASFV)の構造
アスファウイルス科アスフィウイルス属(Asfarviridae Asfivirus)に分類される唯一のウイルスである。
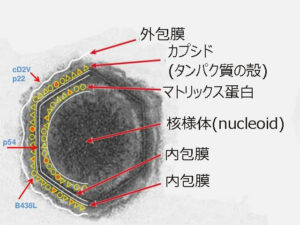
2本鎖DNAをゲノムにもつエンベロープウイルス(ウイルス粒子の外側にウイルスゲノムやカプシドタンパク質を覆う膜状の包みを持っているウイルス)である。
核様体にある直鎖状のゲノムDNAを、①内包膜、②正20面体のカプシド(タンパク質の殻)③外包膜(エンベローブ)の3層で包み込んでいる。
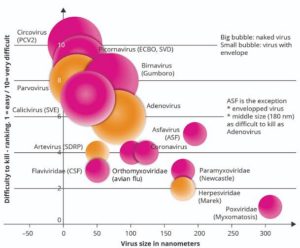
B.巨大なウイルスと血球吸着現象
アフリカ豚コレラウイルス(ASFV)の大きさは260nm程度(1nm=1ナノメートル=1メートルの10億分の1)の正二十面体構造で、同心円状の層が形成されている。
大きなサイズのために、それらを構成するタンパク質のどれが臨床的疾患から保護する抗体を持っているかを発見することが、困難となる。
下記の図は、横軸=ウイルスの大きさ(ナノメートル)と、縦軸=ウイルスを殺す難易度(1=易、10=難)
のポートフォリオである。
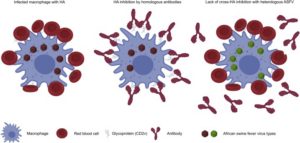
また、アフリカ豚コレラウイルス(ASFV)は血球吸着現象(hemadsorption:HAD)(赤血球凝集能を持つウイルスが細胞内で増殖し、細胞表面にある赤血球が吸着できるようになる現象)をもつ。(遺伝子EP402Rが結合に関与している。)
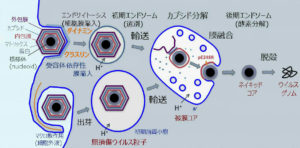
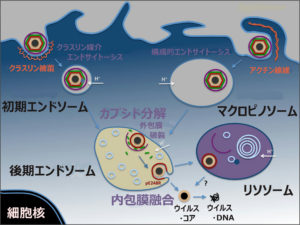
C.ウイルスの侵入から新たなウイルスの複製に至るまでの過程が複雑
アフリカ豚コレラウイルス(ASFV)の侵入から新たなウイルスの複製に至るまでの過程は、次のとおりである。
①ウイルス粒子(ビリオン)
→
②エンドサイトーシス(取り込み、細胞膜の陥入) または マクロピノサイトーシス(細胞外液の取り込み)
→
③ダイナミン(細胞膜からの小胞形成される際の切断に関与)およびクラスリン(エンドソーム外側を形作る骨格となるタンパク質の形成に関与)の仲介
→
④初期エンドソーム(選択、膜の切断・変形、)
→
⑤輸送
→
⑥後期エンドソーム(カプシド分解、内包膜とエンドゾーム膜との膜融合、酵素分解)
→
⑦ウイルス工場で新らしいウイルス粒子(ビリオン)が合成
→
⑧ネイキッド・コア
→
⑨脱殻
→
⑩ウイルス・ゲノム
ASFVは、ダイナミンおよびクラスリンを介したエンドサイトーシスおよびマクロピノサイトーシスを含む複雑なプロセスを経て宿主細胞に入る。
その後、ASFVはエンドサイトーシス経路を進行し、成熟したエンドソーム区画に到達する。
そこで、ウイルスのキャプシド除去と内部ウイルスエンベロープとエンドソーム膜の融合が起こる。
新しく合成されたビリオンは、ウイルス工場で組み立てられ、細胞膜でのエキソサイトーシスの出芽により、またはアポトーシス小体の形成により、細胞を出る。
参考「Endocytosis 」
この過程において、以下「D」に述べる、様々なタンパク質、酵素が、様々な役割を果たしていく。
D.様々な数と種類の構造タンパク質、それらをコードする遺伝子との結びつき関係が多様すぎる
アフリカ豚コレラウイルス(ASFV)は、通常のウイルス粒子(ビリオン: virions)に比して、タンパク質の数が多い。
通常の典型的なウイルス粒子は10〜12個のタンパク質を持っているのに対して、アフリカ豚コレラウイルス(ASFV)粒子には150から200を超える異なるタンパク質があり、それらが、いくつかの層に配置されている。
そのうちの45が既知の構造タンパク質(structural protein)であり、未知の構造タンパク質が23ある。
その他、100を超す非構造タンパク質(unstructural protein )と未分類タンパク質(unassigned protein)または未同定タンパク質( uncharacterized proteins)がある。
これらは、異なる遺伝子からのエンコードによって、それぞれ異なった役割を果たしている。
代表的な構造タンパク質としては、次のものがある。
(A)前駆体蛋白由来生成の成熟タンパク質(前駆体蛋白「」pp220とpp62」由来生成の成熟タンパク質)
アフリカ豚コレラウイルス(ASFV)には、110個のORF(転写後、翻訳されてタンパク質ができる領域)がある。
このうち、前駆体蛋白の「pp220」と「pp62」とをエンコードする二つのORFがあり、この二つの領域で、成熟したタンパク質が生成される。
a.前駆体蛋白「pp220」由来のタンパク質
前駆体蛋白「pp220」 はCP2475L遺伝子によりコードされ、コードされたSUMO様プロテアーゼS273Rによつて切断され、成熟したタンパク質である「pp220由来タンパク質」を産生する。
これらの産生された成熟タンパク質は、それぞれ、ウイルス感染に重要な役割を果たしている。
ウイルスの付着、侵入、複製、免疫応答、キャプシド形成などが、その役割である。
「pp220」由来タンパク質としては
「p5」
CP2475L遺伝子によりコード。Alí Alejo等が2018年に新たにASFVとして 44個の新しいウイルスタンパク質を同定した中の一つ。
参考「A Proteomic Atlas of the African Swine Fever Virus Particle.」(Alejo A、2018年)
「p14」
CP2475L遺伝子によりコード。キャプシド形成、膜構造組み立てに関与。
「p34」
CP2475L遺伝子によりコード。「p150」とともに、膜結合、マトリックス形成に関わっていると見られている。
「p37」
CP2475L遺伝子によりコード。タンパク質の核内輸送に関わっており、シャトルタンパク質と見られている。ウイルス粒子の移動、複製に関与。感染初期では分散した領域にみられるが、感染後期では、細胞質にのみ偏在。
「p150」
CP2475L遺伝子によりコード。「p34」とともに、膜結合、マトリックス形成に関わっていると見られている。
がある。
b.前駆体蛋白「pp62」由来のタンパク質
前駆体蛋白「pp62」は、CP530R遺伝子によりコードされ、コードされたSUMO様プロテアーゼS273Rによつて切断され、成熟したタンパク質である「pp62由来タンパク質」を産生する。
これらの産生された成熟タンパク質は、それぞれ、ウイルス感染に重要な役割を果たしている。
ウイルスの付着、侵入、複製、免疫応答、キャプシド形成などが、その役割である。
「pp62」由来タンパク質としては
「p8」
CP530R 遺伝子によりコード。「p5」と同じく、Alí Alejo等が2018年に新たにASFVとして 44個の新しいウイルスタンパク質を同定した中の一つ。
「p15」
CP530R遺伝子によりコード。キャプシド形成、膜構造組み立てに関与。
「p35」
CP530R遺伝子によりコード。キャプシド形成、膜構造組み立てに関与。
(B)抗原タンパク質「p54とp30とp72」
a.「p54」
E183L遺伝子によりコード。抗原タンパク質。ウイルス侵入に対し、抗原性が高い。ウイルスの成長と、特異抗体の誘導に、重要な役割を果たしている。中和抗体誘導に関与。
b.「p30」
CP204L遺伝子によりコード。抗原タンパク質。ウイルス侵入に最も抗原性の高い構造タンパク質。ウイルス感染後、2~4時間後の早期に発現し、感染サイクルの終始持続。中和抗体誘導に関与。
c.「p72」
B646L遺伝子によりコード。抗原タンパク質。免疫原性(抗原が抗体の産生や細胞性免疫を誘導する性質)が高い。ウイルス二十面体の構造維持に関与。核酸の周囲を包む蛋白の殻(
(C)糖タンパク質「CD2v」
CD2v(like)(EP402R遺伝子によりコード。糖タンパク質。細胞間接着、病原性の強化、免疫応答の調節に関与。免疫回避に役割。リンパ球の機能損傷に関わり合っており、ウイルス感染の広がりを確認するのに重要な役割。感染後期にTおよびNK細胞に発現。
(D)その他の主要タンパク質
a.「p10」
K78R遺伝子によりコード。ウイルスの吸着とウイルス粒子の移動に役割。核への移入に大きな役割を果たしている。一本鎖または二本鎖のDNA結合能力を持つ。
b.「p12」
O61R遺伝子によりコード。宿主細胞へのウイルスの付着に関与している。ウイルス感染の後期に形成。膜表面のタンパク質はウイルスの受容体として機能している。
c.「p14.5」
E120R遺伝子によりコード。DNA結合タンパク質。ウイルス粒子の移動に役割。ウイルス感染の後期に形成。
d.「p17」
D117L遺伝子によりコード。ウイルスの内包膜に定在する膜貫通型タンパク質。
参考
「African Swine Fever Virus Gets Undressed: New Insights on the Entry Pathway」(Germán Andrés 、2017年)
「A comparative review of viral entry and attachment during large and giant dsDNA virus infections」(Haitham Sobhy 、2017年)
(参考)
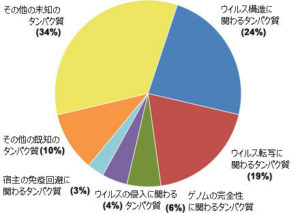
アフリカ豚コレラウイルス(ASFV)ウイルス粒子(ビリオン)( virions )にある構造タンパク質(68)の機能別分類一覧(カッコ内は、塩基配列をアミノ酸に翻訳し構造タンパク質を産生する遺伝子の名前)
ウイルスの構造と形態形成に関わるもの(16)
p5(CP2475L), p8 (CP530R) , p14(CP2475L), p15(CP530R) , p17(D117L), p30(CP204L、P32と同じ), p34(CP2475L), p35(CP530R), p37(CP2475L), p49(B438L), p54(CP204L), p72(B646L), p150(CP2475L),
pS273R(S273R), pE183L(E183L), pE120R(E120R ), p10(K78R), pA104R(CecA1)
ウイルス転写およびRNA修飾に関わるもの(13)
pB962L, pD1133L, pNP1450L, pEP1242L, pG1340L, pQ706L, pNP868R, pC475L, pH359L, pD205R, pD339L, pEP424R, pC147L
ゲノムの完全性維持に関わるもの(4)
pO174L, pNP419L, pE296R, pE165R
ウイルスの侵入に関わるもの(3)
p12(O61R), pE248R, pE199L
宿主の免疫回避に関わるもの(2)
pEP402R 、pA224R
その他の既知タンパク質(7)
pR298L, pB119L, p22(KP177R)(表面抗原タンパク質),p32(p30と同じ)(CP2041L),p11.5(A137R), pEP152R, pH339R
その他の未知タンパク質(23)
pM1249L, pCP123L, pC129R, pC717R, pI177L, pK145R, pK421R, pE146L, pF317L, pH240R, pCP312R, pE423R, pE184L, pC257L, pH171R, pB117L, pB169L, pEP84R, pI73R, pC122R, pQP383R, pM448R, pH124R
合計68
参考
「A Proteomic Atlas of the African Swine Fever Virus Particle」(Alí Alejo、2018年)
「Subunit Vaccine Approaches for African Swine Fever Virus」(Natasha N. Gaudreault ほか、2019年)
「Roles of African Swine Fever Virus Structural Proteins in Viral Infection」(Ning Jia ほか、2017年)
「Antigenic characterization of African swine fever virus (ASFV) p30 and p54 proteins」(Vlad Petrovan、2019年)
以上に見たように、これらのタンパク質の多さと、それぞれのタンパク質への遺伝子からのエンコードの複雑さ、抗原の多様性、免疫回避経路の複雑さ、防御免疫応答を誘導するウイルス抗原の特定の困難さ、などが、アフリカ豚コレラウイルス(ASFV)ワクチンの開発を困難なものにさせている。
E.数多い遺伝子型
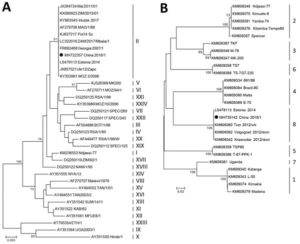
(A)三種類もある遺伝子型配列クレード(系統樹)
アフリカ豚コレラウイルス(ASFV)の遺伝子型の系統樹は、以下3つの抗原タンパク質に基づく遺伝子型クレード(clade)決定のアプローチがある。
「P72 squencing」
「P54 sequencing」
「P30 sequencing」
「P72 sequencing」は、遺伝子「B646L」によつてコードされている「p72タンパク質」の「C末端の配列」を使用しての分類であり、24のクレード(clade)がある。
「P54 sequencing」は、遺伝子「 E183L 」によってコードされている「p54タンパク質」の「全長配列」を使用しての分類であり
「P30 sequencing」は、遺伝子「CP204L」によつてコードされている「p30タンパク質」の「全長配列」を使用しての分類である。
3つのクレード(clade)を対比すると下記のとおりであり、三者の分類の違いは、下記表に見るように、殆どない。
一般的には、「P72 sequencing」によるクレード゛分類がされている。
「P72 sequencing」によるASFVのクレード゛分類は下記のとおりである。
24の遺伝子型が同定されている。
アフリカ豚コレラウイルス(ASFV)の遺伝子型の判定においては、一部のウイルスに識別可能な血清型が欠落しているものがあるため、それについては、24の遺伝子型を識別するP72タンパク質のc末端の配列を使用し、野外株を遺伝子型に分類している。
東アフリカの配列で完全に保存されているのは、塩基(ヌクレオチド)配列で183.3%、アミノ配列で14.2%だった。
遺伝子型をⅠ型(下記図A、24種類の遺伝子型)とⅡ型(下記図B、8種類の遺伝子型)に分け、Ⅰ型は、P72タンパク質のC末端の配列を使用し、Ⅱ型は、野外株を遺伝子型に分類している。
アフリカ西部で分離される株は、主にⅠ型、サルジニア分離株はⅠ型、南東アフリカでの流行株はⅡ型、コーカサス地方、東欧、ロシアで分離された株はⅡ型、最近の中国での流行株はⅡ型に分類されている。
なお、コンゴ西部と南東部で、2つの異なる遺伝子型が見つかっている。
(B)クレード(clade)(系統樹)決定の手順
クレード(clade)(系統樹)決定の手順を平たく言えば次のようになる。
①遺伝情報
DNAに保管。
↓
②転写
RNA 塩基(A、U、G、Cのどれか)を運んで塩基対を作る→DNA の塩基配列を相補的に写し取った RNA を合成→合成された RNA はタンパク質を合成する“指令”を写し取った メッセンジャー RNA(蛋白質に翻訳され得る塩基配列情報と構造を持ったRNA)であり、mRNA と呼ばれる。
↓
③スプライシング
DNA から転写された mRNA にはタンパク質設計に関する部分(エキソン)とタンパク質設計に不要な部分(イントロン)がある。
これからイントロンを除去し、エキソンを繋ぎ合わせる。
↓
④翻訳
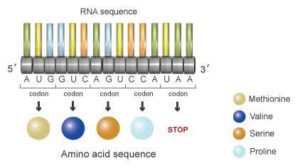
mRNAは4種類の塩基(コドンという)(アデニン(A)、グアニン(G)、シトシン(C)、ウラシル(U)、)の配列情報を持つ。
この内の3 個1組の塩基(コドン)で1個のアミノ酸を作る。
塩基(コドン)には「開始コドン」と「終始コドン」がある。
開始コドン(AUG)はDNAのどこから翻訳するかを決定する。
終始コドン(UAA、UAG、UGG)の直前で翻訳は終了する。
翻訳では、
開始コドンを起点として、その後、3 つの組の塩基づつ、一つのコドンとして遺伝
情報は読まれていく。
↓
⑤アミノ酸への翻訳からタンパク質合成へ
mRNAをアミノ酸に翻訳していくのには、次の過程をたどる。
「アデニン(A)、グアニン(G)、シトシン(C)、ウラシル(U)」の配列の内の3つの組み合わせで、一つのアミノ酸が記号される。
たとえば
「アデニン(A)、グアニン(G)、シトシン(C)、ウラシル(U)」の配列が「AUGGUCAGUCCAUAA」の場合、これを3つ一組のアミノ酸に翻訳すると
「メチオニン(AUG)→バリン(GUC)→セリン(AGU)→プロリン(CCA)→ストップ(STOP)(UAA)」となり、これによって、形成されるたんばく質が決まる。
転写された mRNA にリボソームが結合し、タンパク質が合成されていく。
参考「African swine fever viruses with two different genotypes, both of which occur in domestic pigs, are associated with ticks and adult warthogs, respectively, at a single geographical site」(Carmina Gallardoほか、2011年)
以上のアフリカ豚コレラウイルスの遺伝子型の多様性が、ワクチン開発の標的をどこに合わすかを混乱させている。
幅広い遺伝子型に、単一のワクチンで対応できる(交差免疫能力(C ross-Protective Capabilities)のある)ワクチン開発が迫られているということである。
参考「遺伝子発現の流れ」
(3)アフリカ豚コレラウイルスの免疫回避の動き
A.不十分な中和抗体生成への誘導と発現
中和抗体とは?
中和抗体(neutralizing antibodies)とは、ウイルスの感染を阻止する能力(中和能力)を持つ抗体である。
ウイルスに対して高い結合能(親和性)を持つ抗体がターゲットとする抗原にフラグを立て、中和抗体が中和のための処理をする。
ウイルスの感染能力を阻止する二つの方法
中和能力が発揮されウイルスの感染能力が阻止されるためには、
①中和抗体がウイルスタンパク質に結合し、ウイルスを不活化し、中和能力を発揮する場合
と、
②抗体が間接的に補体(Complement 生体が病原体を排除する際に抗体および貪食細胞を補助する免疫システム (補体系) を構成するタンパク質)を活性化し、ウイルスのたんばく質の受容体結合を阻止したりすることで、結果として、中和能力を発揮する場合
とがある。
通常は、ウイルスが宿主(ASFVの場合は、豚やイノシシ)に感染することによつて、宿主が本来持つている自然免疫系が活性化され、続いて、獲得免疫が誘導され、中和への処理がはじまる。
あるいは、タンパク抗体である中和抗体そのものを宿主に投与することによって、受動免疫ができ、中和への過程が始まる。
アフリカ豚コレラウイルス(ASFV)には通用しない
ところが、アフリカ豚コレラウイルス(ASFV)に対しては、このシステムが、うまく機序しない。
中和能力発揮には次がある。
①抗体は血液や粘膜に分泌され、そこで病原体や毒素などの異物に結合し不活性化(中和)する。
②抗体は補体系の活性化(Complement recruitment)によって、溶解(細胞壁に穴を開ける)により細菌細胞を破壊する。
③抗体が活性細胞や病原体に結合し、その抗体がエフェクター細胞(マクロファージ(白血球の1種でアメーバ様運動する遊走性の食細胞)やNK細胞(自然免疫の主要因子として働く細胞傷害性リンパ球の1種)などの免疫細胞)を呼び寄せ、その抗体が結合している細胞や病原体を殺傷する。
ADCC(Antibody-Dependent-Cellular-Cytotoxicity : 抗体依存性細胞傷害)活性ともいう。
抗体がCDC(Complement-Dependent Cytotoxicity : 補体依存性細胞傷害)活性細胞や病原体に結合し、補体を介して細胞や病原体を殺傷する場合もある。
まったく中和抗体誘導ができないのではない、不十分なのだ
アフリカ豚コレラウイルス(ASFV)のウイルス・タンパク質には、中和抗体誘導が働かないために、このことが、ワクチン開発に支障があるとされてきた。
しかし、まったく中和抗体誘導が働かないというわけではない。
ASFVの構造タンパク質で、中和誘導を目的とするタンパク質としては、次のものがノミネートされる。
(カッコ内はコードする遺伝子名)
p72(B646Lp),とp54(E183Lp)に対する抗体は、ウイルスの細胞への付着を阻害する。
p30(CP204Lp)に対する抗体は、ウイルス取り込みを阻害する。
その他のタンパク質で細胞の表面または、細胞の包膜にあるタンパク質(CD2v、p12, p17)は、ウイルスの侵入や拡散を防ぐことで、中和の役割を果たしている。
いくつかのウイルスタンパク質は、潜在的なワクチン標的として同定されている。
すくなくとも、抗原タンパク質であるP30、P54、P72 、pp62、CD2vは、中和抗体を誘導することができるとされている。
中和抗体を誘導する可能性のあるタンパク質としては、これら抗原タンパク質であるP30やp54やp72に加え、3つの他の抗原関連タンパク質(pEP153R(C型レシチン)、pCP204L(C型レシチン)およびpEP402R(グリコシル化))もあげられうる。
さらに、合計62の膜タンパク質についても、抗原関連のタンパク質であることが同定されている。
しかし、これらのタンパク質に対する抗体は、アフリカ豚コレラウイルス(ASFV)のウイルス複製から保護するのには十分ではないとされている。
ある実験例では、中和抗体を誘導できるCD2vタンパク質でワクチン接種した3頭の豚について、1頭は中和活性を示したが、2頭はウイルス血症にみまわれたとされている。
また、p54とp30をともに接種の場合、臨床症状の発症が遅れ、ウイルス血症が減少し、6頭の豚のうち、E75株による毒性攻撃から保護されたという。
しかし、いずれの場合も、最終は死亡に至ったと言う。
一定の臨床症状の出現の遅れとウイルス血症のレベルの低下は見られたが、最終結果は、すべての豚の死亡を見た。
完全な中和抗体はないが、一定の効果を示す抗体はある、ということなのだろう。
ASFV感染から回復した数少ない例
一方で、ASFV感染から回復した数少ない例においては、一定の防御免疫応答を得ていることも、事実である。
たとえば、米国農務省設立のプラム島動物病センターで、ドミニカ共和国検出のASFV株を用いた接種実験によれば、ウイルス接種による生体実験から回復した豚を3つのグループに分け、急性感染から回復した後の血液中のウイルスの持続性を調べところ、第一グループでは、感染後30日間ウイルス血症が検出。第二・第三グループでは、最初の接種後30日間は低レベルのウイルス血症が検出されたが、その後は検出されなかったという。
この実験例以外にも、これまで、数多くの感染実験において、生存した感染豚の例は確認されている。
これらの各例については
「Lack of evidence for long term carriers of African swine fever virus – a systematic review」(KarlStåhl 、2019年)
をご参照。
最近(2018年と2019年)の例としては
「No evidence for long-term carrier status of pigs after African swine fever virus infection」(Petrov 、2018年)
「Transmission of African Swine Fever virus via carrier (survivor) pigs does occur」(P.L.Eblé ほか、2019年)
があげられる。
これらの事実は、中和抗体をまったく誘導できないという説とは矛盾した事実である。
少なくともタンパク質p54、p30およびp72は、抗体によって媒介されるASFV中和誘導に関与してはいるのだろう。
p54タンパク質は、ASFVを部分的に中和する抗体を誘導しうる。
p72 およびp54 に対する抗体は細胞へのウイルス結合を阻害しうる。
p30 に対する抗体はウイルスの内在化を阻害しうる。
CD2v 、p12、p17タンパク質など、ウイルス粒子の表面に存在するタンパク質は、ウイルスの侵入または拡散を防ぐことで、中和を支援しうる。
ワクチン開発戦略のターゲットを変える必要がある
以上のことから言えそうなのは、、中和抗体だけではASFV感染豚を守ることはできないが、抗体依存性細胞傷害性のある抗体の誘導または血液吸収の阻害、細胞性免疫応答など、他のメカニズムを動員すれば、総体としての中和の力は増すであろうということだ。
これまでのワクチン開発のアプローチ方法では、抗体が直接、ウイルスタンパク質に結びつき、ウイルスの不活性化を試みる方法のみ模索してきたか、今後の動きとしては、それのみだけでなく、抗体遺伝子を活用した受動免疫法に基づく、ワクチン開発も、試行され始めてきている。
しかし、それでも、アフリカ豚コレラウイルス(ASFV)は、以下に述べる免疫応答回避という手法で立ち向かってくる。
B.免疫応答回避のための機序(evasion mechanisms)
Aに見たように、中和抗体の生成が不十分であれば、その不十分さを補完する機序が働くはずであるが、それさえも、ASFVにより阻害されている。
その主な要因は下記のとおりである。
(A)アップ・レギュレーションとダウン・レギュレーション
アップ・レギュレーション(up regulation)とは、応答能が増大することであり、物質や信号が減少することで、受容体の数が増加したり、感受性が過敏になったりして生じる。上方制御、上方調節ともいう。
ダウン・レギュレーション(down regulation)とは、過度,または継続的な刺激によって細胞の応答能が低下(脱感作)することで.受容体数が減少したり、発現量が減少して,応答能が低下することをいう。
アフリカ豚コレラウイルスは、このアップ・レギュレートとダウン・レギュレートの二つをうまく使い分けて、免疫応答の回避をおこなっている。
参考「Mechanisms of African swine fever virus pathogenesis and immune evasion inferred from gene expression changes in infected swine macrophages」(James J. Zhu ほか、2019年)
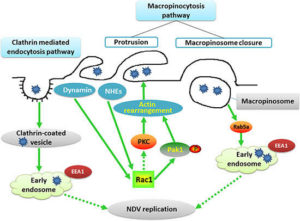
(B)アフリカ豚コレラウイルス(ASFV)侵入経路での免疫回避の動き
アフリカ豚コレラウイルス(ASFV)の細胞への侵入過程は、すでに「2-(2)C」に見たように、次のような過程をたどる。
ウイルスの侵入過程
細胞への侵入には、二つの方法があり
①アクチンを必要とするクラスリン依存性エンドサイトーシス経由(細胞膜の陥入)
②アクチン、キナーゼを必要とするマクロピノサイトーシス経由(細胞外液の取り込み)
がある。
時間的経過で見ると、次のようになる。
①ASFVが、
MHCクラスII抗原(MHCという糖タンパク質)の
処理(細胞内への取り込み→小胞とリソソームが融合→細胞外抗原由来ペプチド生成→小胞体移動)
および
提示(細胞表面に抗原提示)を阻害(邪魔 、Inhibition)
をする。
②
CD8 + Tエフェクター細胞および好中球細胞外トラップを回避。
結果、自然免疫応答および適応免疫応答の両方を回避。
③マクロファージのM1活性化が抑制
④免疫抑制へサイトカイン誘導
⑤マクロファージのオートファジーとアポトーシスのプロセスが阻害。
の流れとなる。
参考
「African swine fever virus-cell interactions: From virus entry to cell survival」(Alonso C ほか、2013年)
「African Swine Fever Virus Undergoes Outer Envelope Disruption, Capsid Disassembly and Inner Envelope Fusion before Core Release from Multivesicular Endosomes.」(B Hernáez、2016年)
以下、免疫関係の用語については、こちらのサイト「免疫」もご参照
a.サイトカインの放出
アフリカ豚コレラウイルス(ASFV)に感染した豚は、高熱、出血性病変、チアノーゼ、食欲不振、などの臨床症状を示し、そして死亡する。
アフリカ豚コレラウイルス(ASFV)がターゲットにしている宿主の細胞は、単球(monocytes)と、マクロファージ(macrophages)である。
単球は、最も大きなタイプの白血球であり、常にマクロファージを補充、マクロファージ(M1、M2)や樹状細胞(DC)( 抗原提示を行う)に分化しうる。
マクロファージは、白血球の1種であり、生体内をアメーバ様運動する遊走性の食細胞であり、掃除屋である。
マクロファージは抗原を摂取すると、各種のサイトカイン(cytokine) を放出し、特定のT細胞(リンパ球の一種で、骨髄で産生された前駆細胞が胸腺での選択を経て分化成熟したもの。)を活性化させる。
これらの放出こそが、アフリカ豚コレラウイルス(ASFV)に感染した豚が臨床症状として示す劇症性のゆえんである。
マクロファージによる抗原提示(食作用によって取り込み、分解した異物を断片にして細胞表面に表出させる)のシグナルを受けて、T細胞のなかのヘルパーT細胞と呼ばれるリンパ球に伝達され、T細胞活性化で、インターロイキンやリンフォカイン等のサイトカインを生産・放出する。
ある種のサイトカインは単球の成熟を促進し、マクロファージを増殖させ食作用を活性化する。
サイトカインはタンパク質で、炎症性のサイトカインと抗炎症性のサイトカインとがある。
①炎症性サイトカイン(inflammatory cytokine)
TNF-α、IL-1、IL-1β、IL-6、IFNγ、IL-8、IL-12、IL-18、G-CSF など
炎症症状を引き起こす原因因子で、活性化マクロファージや活性化血管内皮細胞から産生
②抗炎症性サイトカイン(Anti-inflammatory Cytokines)
IL-4, IL-10, IL-13, TGFβ、TNF-α、IL-1β、IL-6、IFNγ、IL-8、G-CSF など
炎症症状を抑制する働きをもつサイトカインで、活性化マクロファージなどから産生
以下が、主なサイトカイン遺伝子である。(発現レベルの高い順)
IL1RN、TNFSF13B、IL18BP、IL1B_2、IL16、LTB、TNFSF11、CSF3、IL27、TNFSF15、TNFSF10、IL10、IL17F、TNF、IL1A、IFNG、IL1B_1 1.4、IL1A、TNFSF18、TNFSF4,
(その他、発現レベルの弱いものとして IL13、FASLG、LTA、IFNA、IFNB、IFNB)
アフリカ豚コレラ(ASF)の臨床症状を示すサイトカイン因子としては、次のものがある。
FASLG、LTA、LTB、TNF、TNFSF4、TNFSF10、TNFSF13B、TNFSF18
炎症性サイトカイン(IL17Fおよびインターフェロン)や抗炎症性サイトカイン(IL10)は、過剰な組織炎症反応を引き起こす可能性があるとされている。
参考
「Mechanisms of African swine fever virus pathogenesis and immune evasion inferred from gene expression changes in infected swine macrophages」(James J. Zhu ほか、2019年)
b.ケモカインの放出
ケモカイン(Chemokine)も放出するが、これもサイトカインの一種であり、Gタンパク質共役受容体を介してその作用を発現する塩基性タンパク質であり、白血球などの遊走を引き起こし炎症の形成に関与する。
ケモカインもウイルスのレギュレーションを受ける。
ウイルス感染により、
ケモカインCCL2、CCL3L、CXCL2およびケモカイン受容体CCR1、CCR5、CXCR3、CXCR4のmRNAレベルがダウン・レギュレーション(応答能力低下)され、
逆に、
CCL4、CXCL10およびケモカイン受容体CCR7のmRNA発現がアップ・レギュレーション(応答能力増大)される。
参考「Modulation of chemokine and chemokine receptor expression following infection of porcine macrophages with African swine fever virus」(Emma Fishbourne ほか、2013年)
c.アポトーシスの阻害と、オートファジーの阻害
ASFVにとって、アポトーシス (apoptosis) (細胞の自然死)とオートファジー(autophagy)(自食作用)という早期段階での細胞死を防ぐことが、その後の過程におけるウイルスの複製を増やすことにつながる。
ASFVは、ミトコンドリアのカスパーゼ9、カスパーゼ12、エグゼキューターカスパーゼ3の活性化を誘導する。(アップ・レギュレーション)
このウイルスは、いくつかのアポトーシス阻害遺伝子(A238L、A224L、EP153R、DP71L、A179L)をコードしている。
これらの機能は、ウイルスの複製を損なう可能性のある早期細胞死を防ぐためにある。
参考「African Swine Fever Virus Inhibits Induction of the Stress-Induced Proapoptotic Transcription Factor CHOP/GADD153」(Christopher L. Netherton、2004年)
アポトーシス・レギュレーターたんばく質のBcl-2(遺伝子LMW5-HL)の相同体であるA179Lが、宿主細胞のアポトーシスを抑制(ダウン‐レギュレーション)し、複製ウイルス産生を促進させる。
参考「The modulation of autophagy by African swine fever virus」(Gareth Shimmon ほか、2019年)
d.好中球の発現とリンパ球&単球
好中球(neutrophil)は5種類ある白血球の1種類である。
盛んな遊走運動(アメーバ様運動)を行い、主に生体内に侵入してきた細菌や真菌類を貪食(飲み込む事)することで、感染を防ぐ役割を果たしている。
アフリカ豚コレラウイルス(ASFV)は、次のような遺伝子の差次的発現によって、ダウンレギュレートをしている。
(i)MHCクラスII抗原の処理および提示を阻害し、
(ii)好中球/ CD8 +の発現を減少させることにより
CD8 + Tエフェクター細胞および好中球細胞外トラップを回避し、自然免疫応答および適応免疫応答の両方を回避
(iii)マクロファージのM1活性化の抑制
(iv)免疫抑制サイトカインの誘導
(v)マクロファージのオートファジーとアポトーシスのプロセスの阻害。
とのダウンレギュレーション効果を発現している。
参考「Mechanisms of African swine fever virus pathogenesis and immune evasion inferred from gene expression changes in infected swine macrophages」(James J. Zhu ほか、2019年)
e.膜融合( membrane fusion)の阻害
ノコダゾール(nocodazole)は、ウイルスが微小管(microtubules)を通じて原形質膜(plasma membrane)に向かい順行性輸送されることによるウイルスの複製機能強化を阻止する役割を持つている。
そのノコダゾールの機能を、PI3キナーゼ(ホスファチジルイノシトール3キナーゼ)が阻害することで、ウイルスの複製を助けている。(ダウン‐レギュレーション)
参考「Transport of African swine fever virus from assembly sites to the plasma membrane is dependent on microtubules and conventional kinesin.」(Jouvenet Nほか、2004年)
f.転写活性体の応答低下
A238Lpは、宿主の免疫応答遺伝子の転写活性化を防ぐ働きをする。(ダウン‐レギュレーション)
また、アポトーシス促進転写因子(CHOP / GADD153)はストレス誘発性の機能を持ち、アポトーシスへの誘導を阻害する。
A238LpはNF-κappaB(転写因子であり、遺伝子転写を活発化)を阻害(ダウンレギュレーション)する蛋白質でもある。
参考「Mechanism of Inactivation of NF-κB by a Viral Homologue of IκBα
SIGNAL-INDUCED RELEASE OF IκBα RESULTS IN BINDING OF THE VIRAL HOMOLOGUE TO NF-κB*」(Stephen W. G. Tait ほか、2019年)
g.インターフェロンの働き
インターフェロン (IFNs)には、Ⅰ型Ⅱ型Ⅲ型の三種類がある。
ウイルスなどの異物の細胞への侵入に反応して細胞が分泌する蛋白質である。
このうちⅠ型インターフェロンは、更に五種類に分かれ、「IFN-α(13種類)、IFN-β(1種類)、IFN-ω(1種類)、IFN-ε(1種類)、IFN-κ(1種類)」がある。
アフリカ豚コレラウイルス(ASFV)には、このうち、IFN-βが、一定の役割を果たしている。
IFN-βは、ウイルス攻撃に応答する線維芽細胞や様々な細胞から産生される。
IFN-β はBリンパ球ミエローマ細胞(免疫グロブリンを大量に産生)においてアポトーシス効果を選択的に誘導させる。
参考「African swine fever virus Armenia/07 virulent strain controls IFN-β production through cGAS-STING pathway」(Raquel García-Belmonteほか、2019年)
h.シグナル伝達(signaling pathway)の阻害
I329Lpタンパク質は、宿主細胞の表面膜に局在する糖タンパク質である。
I329Lpタンパク質は、Toll様受容体3(TLR3)シグナル伝達経路において、IFN応答を阻害する。(ダウン‐レギュレーション)
参考「Analysis of the african swine fever virus immunomodulatory proteins
Article」(Mariia Nefedevaほか、2019年)
また、シグナル回路において、A238Lpたんばく質は誘導型一酸化窒素合成酵素(iNOS)による遺伝子発現を阻害(ダウン‐レギュレーション)し、マクロファージによる強力な抗炎症効果を発揮させる。
参考「Regulation of Inducible Nitric Oxide Synthase Expression by Viral A238L-Mediated Inhibition of p65/RelA Acetylation and p300 Transactivation」(Aitor G. Granjaほか、2006年)
i.リン酸化酵素によるウイルス核内移行の促進とサイトカイン等の産生促進
パターン認識受容体であるcGASが環状GMP-AMPを合成し、この環状GMP-AMPが小胞体に局在する膜貫通型タンパク質(STING)に結合する。
STINGはC末端側でリン酸化酵素TANK binding kinase 1(TBK1)と結合し,TBK1を活性化させる。
活性化したTBK1は、同時にSTINGはSTINGおよび転写因子(IRF3)をリン酸化し、IRF3の核内移行を促進させる。
核内移行の転写因子(IRF3)で、,抗ウイルス活性を有するI型IFNや炎症性サイトカインであるinterleukin-6やTNFの産生が誘導される。(アップ‐レギュレーション)
参考
「Inhibition of cGAS-STING-TBK1 signaling pathway by DP96R of ASFV China 2018/1.」(Wang Xほか、2018年)
j.MHCクラスI抗原の表面発現の阻害
MHC(主要組織適合性複合体)は、細胞表面に発現している糖タンパク質で、自己と非自己(外来の細菌やウイルス)を識別し、免疫反応を開始できる。
MHCには、タンパク質の機能や構造の違いで3つに分けられ、クラスI、クラスII、クラスIII の遺伝子領域に分類されている。
アフリカ豚コレラウイルス(ASFV)のレクチンEP153Rは、MHCクラスI抗原の表面膜発現を選択的にダウンレギュレーションする。
EP153Rは、エキソサイトーシスプロセス(Exocytosis)(細胞内分泌物質を細胞外に開口分泌するプロセス)を損傷することで、MHC抗原の合成またはグリコシル化に影響を与えることなく、MHC-I膜発現を阻害する。
MHCクラスII抗原の処理および提示についても阻害がある。
k.樹状細胞によるサイトカイン応答調整
樹状細胞( Dendritic cell=DC)は、抗原提示細胞として機能する免疫細胞の一種である。
ASFVはサイトカイン応答の誘発を防ぐ調整をしている。
弱毒株と強毒株によってマクロファージサイトカイン応答が異なるアップまたはダウンのレギュレーションをしている。
(「a.サイトカインの放出」もご参照)
参考
「Modulation of MHC class I expression by African swine fever virus and the role of virus proteins EP153R and CD2v」(Deborah L. Saward Arav、2014年)
「African Swine Fever Virus Causes Microtubule-Dependent Dispersal of the trans-Golgi Network and Slows Delivery of Membrane Protein to the Plasma Membrane」(Christopher L Netherton ほか、2006年)
「The African swine fever virus lectin EP153R modulates the surface membrane expression of MHC class I antigens」(Hurtado C ほか、2010年)
https://www.researchgate.net/publication/47743540_The_African_swine_fever_virus_lectin_EP153R_modulates_the_surface_membrane_expression_of_MHC_class_I_antigens
以上、「(C)アフリカ豚コレラウイルス(ASFV)侵入経路での免疫回避の動き」についての総合的な参考サイトは下記の通り
「Subunit Vaccine Approaches for African Swine Fever Virus」(Natasha N. Gaudreault ほか、2019年)
「Antibody-mediated neutralization of African swine fever virus: Myths and facts」(José M. Escribaほか、2012年)
「Approaches and Perspectives for Development of African Swine Fever Virus Vaccines」(Marisa Arias ほか、2017年)
「African Swine Fever Virus Gets Undressed: New Insights on the Entry Pathway」(Germán Andrésほか、2017年)
「Mechanisms of Entry and Endosomal Pathway of African Swine Fever Virus」(Elena G. Sánchez ほか、2017年)
「Mechanisms of African swine fever virus pathogenesis and immune evasion inferred from gene expression changes in infected swine macrophages」(James J. Zhu ほか、2019年)
3.アフリカ豚コレラウイルスワクチン開発の歴史と現状
以上、これほど以前から世界中に蔓延しているアフリカ豚コレラウイルスであったにも関わらず、なぜ、それに対するワクチン開発が遅れ、そして、今なお、完璧なワクチン開発の目処が立っていないのか?その原因について述べた。
アフリカ豚コレラ(ASF)用ワクチン開発の困難性は、次にあった。
①ウイルス発生のシナリオが、アフリカ、ヨーロッパ、東アジアの三地域で全部異なり、宿主も異なり、遺伝子型もことなっていた。
②ウイルスが巨大で、かつ、その構造も複雑でった。
③ウイルスのたんばく質の種類が多く、また、そのタンパク質をコードする遺伝子の数も多く、その役割も多岐にわたっていた。
④中和抗体の力が十分ではなかった。また、ASFVの複雑な免疫応答回避の機序が未解明であった。
⑤過去にポルトガルでのワクチンの失敗が、その後も尾を引いていた。
⑥ウイルスを扱え、また、遺伝子組み換え実験ができるBSL3/4クラスの研究施設が少なかった。
⑦ワクチン大量生産が出来る細胞株(Cell Lines)生産施設がなかった。
⑧安価に動物実験ができるモデル環境がなかった。
ここで、これまでの、アフリカ豚コレラワクチン開発の苦闘の歴史と、現時点における開発の展望について述べる。
(1)散々な失敗に終わった世界最初のASFVワクチン
アフリカ豚コレラワクチンが世界で最初に使用されたのはポルトガルであった。
ポルトガルは、1957年、ヨーロッパに最初にアフリカ豚コレラウイルスが上陸した最初の地であった。
アフリカ豚コレラウイルスの上陸は、ポルトガルのリスボンの空港近辺で生ゴミで育てられた豚の感染から始まった。
感染源は、アンゴラから空輸で運ばれた感染豚肉製品と推測された。
この最初の蔓延は早期に鎮圧されたのだが、1960年に再び、ポルトガルのリスボンに上陸し、その後、スペインに感染拡大し、その後、1995年まで、感染拡大が続いた。
最初のアフリカ豚コレラワクチンは、感染豚の骨髄で継代培養し弱毒化されたワクチンであり、1963年から、約550,000頭の豚に接種された。
問題は、その後、接種された豚のうちの128,624頭に副作用が出たことであった。
副作用の症状としては、肺炎、流産、運動障害、などであった。
そして、このワクチン接種の結果として、その後、長年にわたり、多くの亜急性・慢性型のアフリカ豚コレラ感染豚を生み出したものと推測されている。
参考
「Vertebrate Animal and Related Viruses」(EDOUARD KURSTAK ほか、1981年)
「Vaccination against ASF」
(J Manso-Ribeiro, JL Nunes-Petisca, F Lopez-Frazao… – Bull Off Int Epizoot, 1963)
(2)その後も続いたASFワクチン開発の失敗
ワクチン開発の模索はその後も続いたが、いずれも、十分の抗体を得ることができずに、失敗した。
ワクチン開発のターゲットは次に絞られた。
①不活化ワクチン(Inactivated vaccines)
抗体形成は誘導されうるが、防御にまでは至らない。
感染ウイルス粒子に二つのタイプ(Intercellular virions(IV)とextracellular virons(EV)と)があることがネック。
不活化に異なった方法と、異なったアジュバント(PolygenとEmulsigenと)がある。
細胞性免疫低下(食細胞、細胞傷害性T細胞の機能低下)あり。
抗体依存性感染増強現象(ADE)(ウイルスが抗体を利用してマクロファージや樹状細胞等の抗原提示細胞に効率よく感染するためのメカニズム)あり。
副作用はないが、ASFVに対する防御効果はない。
②弱毒生ワクチン(Live attenuated vaccines, LAVs)
自然に弱毒化した分離ウイルス株
相同保護効果を、持つ。
異種保護効果は部分的。
ASFVに対する防御効果は、予防接種用量や予防接種ルート(経口か接種か)によって異なる。
ASFVに対する一定の防御効果はあるが、副作用が強い。
副作用として、持続感染(キャリア)や慢性臨床症状がある。
③サブユニットワクチン(Subunit vaccines)
アフリカ豚コレラウイルス(ASFV)の抗原タンパク質をセットにして、宿主域の拡大が出来、発現促進ができる組換えバキュロ
組み合わせのコンビは
P15とP17とp30とP32とP35とp54とP72とP72とCD2vのいずれかの組み合わせ。
P54とP30の組み合わせは感染の遅延などの部分的な効果はある。
P54とP30とP72との組み合わせは、ASFVに対する防御効果はない。
CD2vは感染の遅延などの部分的な効果はある。
DIVAワクチンである。
検出可能な抗体は得られたが、ASFVの防御にまでは至らない。
④DNAワクチン(DNA vaccines)
「遺伝子の運び屋」にプラスミドベクターを使い、これにDNA断片を組み込み、発現。
DIVAワクチン。
細胞傷害性 Tリンパ球(CTL)反応を誘導。
ASFに対する防御効果はまだない。
⑤ウイルスベクター生ワクチン(Live virus-vectored vaccines)
種痘に用いられるワクチニアウイルス(ポックスウイルス科に属するエンベロープを持ったウイルス)を、使う。
アンカラ、アデノウイルス、オーエスキー病ウイルスなど。
細胞傷害性 Tリンパ球(CTL)反応と抗原特異的抗体を誘導。
DIVAワクチンである。
ASFVに対しては、部分的に防御。
⑥組み換え弱毒生ワクチン(Recombinant LAVs)
相同組換えのメリットあり
干渉効果( 近縁なウイルスに感染しなくなる)あり。
副作用(ウイルス血症、残留毒性)がある。
これが、現状では最も有力なワクチンであるが、副作用の問題はまだ克服されていないようだ。
遺伝子から削除(欠失)するタンパク質の候補としては、以下のものが対象となる。
削除(欠失)により劇症性が低下するもの
DP71L,DP96R,
削除(欠失)により相同性(Homologous)があがるもの
9GL,MGFs,DP148R,
削除(欠失)により汎用性(Heterologous)があがるもの
A238L,A224L,
削除(欠失)により交差防御(Cross-protection)効果があがるもの
CD2v,
なお、上記効果はウイルス(ASFV)によって異なる。
以上に見るように、いずれの方法でのワクチン開発も一長一短で、まだ、決定的にアフリカ豚コレラウイルス(ASFV)からの防御をしうるものは、ない。
しかし、近年、ワクチン開発のターゲットが、以下に見るように絞られてきつつはある。
参考「Can a Vaccine Save the World’s Pigs from African Swine Fever?」
(3)中国のASF感染拡大で勢いづく世界のワクチン開発競争
A.潮目が変った、世界のASFVワクチン開発への動き
一昨年、アフリカ豚コレラ(ASF)発生が中国に及んだ時点で、ASFワクチン開発への動きは加速せざるを得なかった。
それまでのアフリカ豚コレラ(ASF)問題は、アフリカや東欧のごく限られた地域での家畜疾病問題に過ぎず、世界のASFワクチン開発への動意は薄かった。
巨額な開発費がかかるASFワクチン開発への資金投入に見合うまでの大きなマーケットがなく、したがってワクチン開発の費用対効果が見込まれなかったからである。
しかし、アフリカ豚コレラ(ASF)感染ステージが上記の第四期に進むにつれ、世界の各地で、アフリカ豚コレラ(ASF)ワクチン開発への動きが激しくなってきた。
「中国でのアフリカ豚コレラの感染拡大は、ASFのワクチン開発にとっては「ゲームチェンジャー」であったという人もいる。
B.各国の動向
中国ではハルビン獣医学研究所で、実験室段階ではあるが、2つのワクチン候補を確定したと発表した。
ベトナムでは、ベトナム国立農業大学で開発されたASFワクチンを、大学実験室とベトナム北部の3つの農場でテストしていると、ベトナム農業大臣グエン・スアン・クオン(Nguyen Xuan Cuong)氏が発表している。
また、ロシアでは、ロシア農業アカデミー委員会が、全ロシアロシア獣医微生物学研究所(VNIIVViM)にASFに対するワクチンならびにこの疾患の新しい効果的な治療および予防ツールを開発する任務を置いたと、発表している。
また、全ロシアロシア獣医微生物学研究所(VNIIVViM)は、イリノイ大学と共同でASFワクチン開発に取り組んでいる。
アメリカでは、1970年代に、ポルトガルとスペインにASFが発生したのを契機に、ASFワクチン研究を開始したが、開発資金上の問題で、2004年に研究を終了していたが、ジョージアでASFが発生したのを機に、研究を2008年に復活した。
ASFの研究で世界的に有名な科学者であるマヌエル・ボルカ(Manuel Borca)氏のリーダーシップのもと、プラム島で研究が再開されている。
昨年、米国国土安全保障省(DHS)科学技術局(S&T)は、米国農務省(USDA)と共同でのワクチン研究を強化し、プラム島を本拠にして、ニューヨーク州動物病センター(PIADC)とも連携し、アフリカ豚コレラタスクフォースを設立した。
イギリスでは、パーブライト家畜衛生研究所(Pirbright Institute)を中心に、現在、弱毒生ワクチンとサブユニットワクチンを開発しているほか、Viro Vet Diagnostik と協力しASF抗ウイルス薬製造に取り組んでいる。
スペインでは、スペインを、代表するバルセロナ自治大学の研究所 CReSA-IRTA で、フェルナンド・ロドリゲス博士(Fernando Rodriguez)主導のもと、いくつかの弱毒化生ワクチンのプロトタイプが成功しているとのことである。
C.現在開発中の世界の研究機関は?
現在、世界で、アフリカ豚コレラ(ASF)用のワクチン開発に踏み切っている研究機関は、少なくとも21機関、10カ国に及んでいる。
その主なものは
フランスー①ANSES,②ORAD,
スペインー①CBMSO-CSIC,②CReSA-IRTA,③INIA-CISA,④VISAVET-UCM,
ドイツーFLI,
ポルトガルー①IGC,②FMV-ULisboa,
イタリアー①IZS-Peruggia,②IZS-Sardegna,
イギリスーPIR,
アメリカー①Vet.Kansas state,②USDA,
ロシアー全ロシアロシア獣医微生物学研究所(VNIIVViM),
中国ー①HVRI,②CHAHEC,③LVRI,④IAS,⑤IMV
ベトナムー①the Vietnam National University of Agriculture、②フランスCevaグループとダバコグループ[DBC](Dabaco)とワクチン生産RTD社との連携、
オーストラリアーthe Australian Animal Health Laboratory (AAHL)
カナダーVIDO-InterVac( Vaccine and Infectious Disease Organization-International Vaccine Centre )
D.現在、アフリカ豚コレラワクチン開発に興味を有している民間企業は?
次の会社と見られている。
①Zoetis,②Ceva,③Lavoratories Calier,③CZ Veterinaria,④MSD Animal Health,⑥Laboratorios Hipra,⑦Boehringer Ingelheim Espania,S.A,⑧IDT Biologika,⑨IMICROQ.S.L,⑩Rekom Biotech,⑪BIOORGANIC RESEARCH AND SERVICES S.L(BIONATURIS),⑫Vacunek.S.L. ⑬Thermofisher, ⑭Aquilon CyL,S.L,⑮IDEXX LABORATORIOS,⑯Laboratorios Larrasa, ⑰CALIER.⑱HIPRA,⑲Yebio,⑳Tecon, ㉑Pulike,㉒CAHIC,
(4)現在、世界で最も有望なASFワクチンはなにか?
A,ワクチン開発のための六条件
いずれのワクチン開発も、現時点では実用化を見込めない状況ではあるが、それらのワクチン開発技術の中での一定の取捨選択は始まっているようだ。
実用化として求められる条件は、次の六点である。
①安全性
弱毒株生ワクチンの中には、強い副作用を伴ったり、亜急性・慢性型の後遺症を残すものもある。
遺伝子欠損を含む遺伝子組み換え弱毒化生ワクチンにおいても、接種後、亜急性・慢性型の後遺症を持つものもある。
②効率性
異なった遺伝子型のASFVに対しても、交差反応が得られる汎用性が求められる。
③安全性と効率性との両立
安全性を確保するために、あまりに弱毒化に重点をおくと、効果がえられず、かと言って、あまりに効果に重点をおくと、副作用が強くなる。
そのへんのバランスを保つことが必要である。
④DIVAワクチンになりうること
接種後のサーベイランスに伴う負担を考えれば、DIVAワクチンである必要がある。
⑤商業生産が可能なこと
その条件として、細胞培養(cell culture)から、培養期間の短い細胞株(cell lines)への転換が必要。
⑥野生イノシシにも使用可能なこと
野生の温度条件や太陽光条件下で、野生イノシシ用に使用しても、効力を失わないワクチンである必要がある。
B.その中での有望な三例
では、現状で、生き残りうるアフリカ豚コレラ(ASF)用ワクチンは、どのようなものなのだろう?
明らかにふるい落されうるのは、古典的な不活化ワクチンであり、次にふるい落されるのは、サブユニットワクチンである。
弱毒化生ワクチンはどうかといえば、自然弱毒化では生き残りは難しく、細胞培養または遺伝子欠失による連続継代により弱毒化した、遺伝子組み換えとのハイブリットでの「遺伝子組み換え弱毒化生ワクチン」としてなら存続しそうだが、ここでも、強い副作用の克服が課題として残っている。
そのような中で、次の二つの有望なワクチン開発動向を紹介しておこう・
(A)スペイン マドリッド・コンプルテンス大学獣医学部での経口ワクチン開発
昨年10月に韓国にアフリカ豚コレラ(ASF)が発生したときに、韓国の新聞「中央日報」に仁荷大学校のキム・ウンギ教授(김은기)が紹介したのがこの研究であった。
この研究は スペイン マドリッドコンプルテンス大学獣医学部のJose A. Barasona等が進めているものである。
今年5月、研究者は野生イノシシから「弱毒ASFウイルス」を分離し、これをイノシシの餌に混ぜて与えたところ、92%に免疫ができたという。
2017年にラトビアで分離された遺伝子II型のASFウイルス株(Lv17 / WB / Rie1)を、弱毒化し、赤血球吸着現象を持たないようにされたもので、そのうちの抗原タンパク質「p72」をワクチン接種に使用した。
このために、遺伝子EP402RからCD2様コーディング配列を削除(欠失)した。
18頭のうち、12頭をBSL-3実験施設に置き、①最初に9頭にワクチン経口接種し、②残りの3頭は、経口ワクチン接種されたイノシシと同居させ、それぞれ同居開始日数を、0日、7日、15日にわけ、暴露接触させた。
経口によるワクチン接種期間は30日間、続いた。
次に新たに、③4頭のイノシシにワクチンの筋肉注射をし、この筋肉注射の30日後に、新たな④2頭のイノシシに接触曝露させた。
こうして、18頭のイノシシに全部、曝露が行き渡るようにし、感染結果を確認した。
①については、9頭のうち、6頭が、接種後15日から18日に抗体陽性、
②については、3頭すべてが、同居接触後、14日から16日に抗体陽性、
となった。
③の抗体獲得後に特異の臨床症状を示したイノシシは、経口ワクチン接種イノシシにはまったくなかったが、筋肉注射による接種のイノシシは、全て、重度の臨床症状を示した。
一方④の③に接触同居したイノシシは③と同様の重度の臨床症状を示したが、③ほどには重症化せずに、その後に回復したイノシシもいたと言う。
以上のことからいえるのは、副作用が少ないという経口ワクチンの優位性は示されたといえる。
また、遺伝子II型を対象としたワクチンとしては、最初のもので、このことは、現在、中国から世界へと蔓延拡大を続けるII型ウイルスに対するワクチンの交差防御性を高めるうえで、意義深いものと思われる。
92%に免疫確保できたということは、副作用を克服すれば、実用化できそうなワクチンではある。
参考「First Oral Vaccination of Eurasian Wild Boar Against African Swine Fever Virus Genotype II」
(B)アメリカ USDA プラム・アイランド動物疾病センターでのワクチン開発
遺伝子組み換え弱毒化生ワクチンの開発において、ウイルスの遺伝子のなにを削除(欠失)すればいいのかは、大きな問題である。
USDAのプラム・アイランド動物疾病センター(Plum Island Animal Disease Center )では、その候補となる遺伝子として「I177L遺伝子」に注目した。
この「I177L遺伝子」については、これまで、ほとんどマークされていなかった。
わずかに、ジョージア州立大学のPeter W. Krugが、2015年に「I177L遺伝子はタンパク質分解のプロセスに関与しているようだが、ASFV病原性におけるこの遺伝子の役割は不明」としている。
「The Progressive Adaptation of a Georgian Isolate of African Swine Fever Virus to Vero Cells Leads to a Gradual Attenuation of Virulence in Swine Corresponding to Major Modifications of the Viral Genome」(Peter W. Krugほか、2015年)
また、昨年、スペインのマドリード自治大学のAlí Alejoらが、「この遺伝子は、ウイルス膜中のタンパク質(Membrane protein)にリンクされている」としていた。
参考「A proteomic atlas of the African swine fever virus particle」(Alí Alejoほか、2019年)
USDAの研究チームは、アフリカ豚コレラウイルス(ASFV)の持つ免疫回避機能に注目し、「では、どの遺伝子を削除(欠失)すれば、ASFVの持つ免疫回避機能を社団できるのか?」に絞り、その候補遺伝子として、次の3つを候補とした。
①EP152R
②L83L
③I177L
このうち、①は必須遺伝子(CCL2vタンパク質をエンコード)であり、削除(欠失)できなかった。
②は結合タンパク質をエンコードしており、削除(欠失)はできたが、ウイルスの毒性には、影響がなかった。
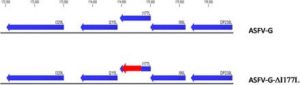
③は後期転写遺伝子であり、逆鎖(左方向へ読み取り)に位置しており、免疫調整タンパク質をエンコードしていると見られ削除(欠失)できた。削除(欠失)と同時に、ウイルスは完全に弱毒化できた。
この「I177L遺伝子を削除(欠失)したワクチン候補を「ASFV–
動物感染実験はUSDAのプラム島動物病センター(PIADC)の施設で、3AGレベルのバイオセーフティーの条件下で行われた。
28日間にわたり5グループの豚をもとに行われた感染実験では、次の結果を示した。
ワクチン接種は筋肉内接種をもって行われた。
接種量を、低用量(102 HAD 50)、中用量(104 HAD50)、高用量( 106 HAD50)に分けた。
用量の高低に関わらず、免疫を獲得できた。
更に、親株の「ASFV-G」(ジョージア分離株)のチャレンジ感染試験においても、免疫が獲得できた。
副作用は、いずれの用量においても、見られなかった。
「ASFV–
ワクチン接種豚と同居のワクチン未接種の豚についても、臨床症状は見られなかった。
今後は、より大きな群れの豚での感染実験を行う予定だと言う。
この「ASFV–
いいことづくめの「ASFV–
問題は、DIVAワクチンとしての商品化が可能かどうか? 野生イノシシにも適用となれば、経口ワクチンとして使えるのか? などなどの課題がある。
商品化までの年数にしても、規制当局の承認までの年数を考えれば、早くて5年以内というのが目安のようだ。
参考
「Development of a highly effective African swine fever virus vaccine by deletion of the I177L gene 2 results in sterile immunity against the current epidemic Eurasia strain.」(Manuel V. Borcaほか、2020年1月)
「Finding the right ASFV gene to delete for a live-attenuated vaccine」
(C)中国の中国農業科学院 ハルビン獣医研究所でのワクチン開発
2019年8月19日、中国農業科学院 ハルビン獣医研究所は、「遺伝子削除弱毒アフリカ豚コレラワクチンウイルスとワクチンとしての応用」という名の特許申請をした。
内容は、
①2018年に黒龍江省で分離されたアフリカ豚コレラウイルス(ASFV)の「Pig/CN/HLJ/2018」(遺伝子バンク登録番号MK333180.1)を親株として、ワクチンを作る。
②ワクチンは、遺伝子削除(欠失)弱毒化ワクチンとする。
③削除(欠失)される遺伝子は二種類あり
a.「MGF360-505R」
b.「CD2v」と「MGF360-505R」
④ワクチンは、二種類の組み合わせとする。
この特許登録の発表に先立って、昨年(2019年)5月24日に、ハルビン獣医研究所から、「ハルビン獣医研究所が独自に開発したアフリカ豚コレラ(ASF)ワクチンが段階的に成果を上げ、ワクチン株培養のシステムも確立し、候補ワクチン株のうちの二つが安全性と免疫保護性を確保した」と発表していた。
感染実験の結果の詳細については明らかにされていないが、次の通りである。
実験用豚にワクチン接種後、実験用豚は100%生存、親株によるチャレンジでは95%以上生存したと言う。
ワクチン接種によって、実験豚には、高レベルのTNF-α、Ⅰ型インターフェロン、特異抗体、細胞性免疫を産生させたとのことである。
これまで、中国におけるアフリカ豚コラワクチン開発は次の4つの戦略目標を元に進められてきた。
①遺伝子削除(欠失)ワクチン
削除(欠失)対象はCD2v,MGF,UK、で、この内の単一または複数の遺伝子削除(欠失)で、毒性をなくすこと
②サブユニットワクチン
p72.p54.p30.CD2vのタンパク質を対象
③DNAワクチン
上記の遺伝子が対象
④ウイルスベクター生ワクチン
PrV/VACV/AdVを対象
これらのこれまでの戦略を、「「CD2v」と「MGF360-505R」の遺伝子を、単一または複数削除(欠失)した弱毒化ワクチン」に集約して、今後取り組むものと思われる。
商品化実現時期については、遺伝子削除(欠失)ワクチンの承認には、二つの手順(動物医薬品承認と遺伝子組み換え安全性評価手順)が伴うため、通常のワクチン承認よりは、長い時間がかかるものと見込まれている。
4.終わりに
以上、アフリカ豚コレラ(ASF)ワクチン開発がなぜ困難で、これからの開発見通しがどうなのか?について述べてきた。
光明は既に見えている。
既にアフリカ豚コレラ(ASF)ワクチンの国別開発は、アメリカ、スペイン、中国に絞られている。
その次に来うるのはベトナムだ。
とくに、実現性が高いのは、アメリカUSDAのワクチン「ASFV–
しかし、そのアメリカにしても、商品化に至るまでは、少なくともまだ5年かかると言う。
ワクチンの種類としては、遺伝子削除(delete)(欠失)弱毒化ワクチンに絞られた感じだ。
この中での、遺伝子の選抜が繰り返されるということになるだろう。
日本でもアフリカ豚コレラ(ASF)ワクチン開発の宣言はされている。
しかし、先進各国にキャッチアップするのは、既に無理だろう。
2020年1月5日記 笹山 登生

の場合、高熱がない 0d-300x72.jpg)
